岩芯分析
引言
核磁共振(NMR)波谱的主要用途之一是对未知化合物进行结构解析,并对已知化合物进行结构确认。
本应用笔记分析了使用牛津仪器宽带台式核磁共振波谱仪X-Pulse获得的一系列一维和二维NMR波谱,显示了如何将通过NMR波谱获得的信息与已知分子的结构特征相对应。在本案例中,我们选择了布洛芬分子,在CDCl3溶液中的浓度为1 mol/L,并记录下它的波谱。
布洛芬
布洛芬,2-(4-(2-甲基丙基)苯基)丙酸,是一种常用于治疗疼痛、发烧和炎症的抗炎药。布洛芬最初于1961年由在英国诺丁汉的Boots UK公司工作的Stewart Adams博士和John Nicholson博士发现。布洛芬已被列入世界卫生组织的基本药物清单,在全球范围内无需处方即可获得。之所以选择它作为例子,是因为它在分子量和结构复杂性方面与广泛的常用生产药物相似,这些药物易于通过台式核磁共振仪进行分析。
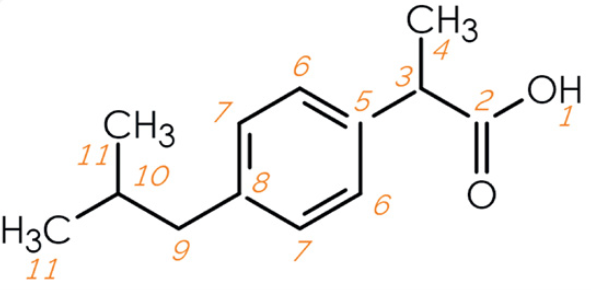
布洛芬的分子结构如图1所示。其中可以清楚地识别出八种独特的质子化学环境(1、3、4、6、7、9-11)和十种独特的碳环境(2-11)。
布洛芬的分子结构如图1所示。其中可以清楚地识别出八种独特的质子化学环境(1、3、4、6、7、9-11)和十种独特的碳环境(2-11)。
结构测定
简单的一维核磁共振谱,需要激发单独一种同位素原子核,从而专门获得有关这些原子的信息。这会产生信号强度对应频率的波谱。化学位移(δ)绘制在水平轴上,单位为ppm(百万分之一)。以ppm而不是赫兹(Hz)为单位绘制化学位移图,可确保不同波谱仪测量的数据之间具有可比性。
大多数已知或未知样品的第一个核磁共振谱,通常会是一个简单的质子(氢-1)核磁共振谱。对于大多数样品来说,仪器可以在5分钟内获得满足结构分析要求的氢谱。布洛芬的1H NMR波谱如图2所示。
核磁共振谱图中的信号包括一个或多个单独的峰。例如,δH 11.9 ppm处的信号是一个单峰,而以δH 3.7 ppm为中心的信号包括四个峰(通常称为四重峰)。对于1H NMR谱图中的每个信号,应考虑三个特征要素:
1. 谱图中信号的化学位移δH,对应于产生信号的原子核的局部化学环境。
2. 每个信号的(积分)面积,对应于与每个信号相关的原子核个数。图2中每个信号下方以绿色来显示积分值。
3. 信号的多重性,包括信号中的峰数、它们的相对强度和各峰之间的间隔,提供了附近其它核磁共振活性核的信息。
 了解更多信息
了解更多信息
在最初仅考虑信号的化学位移和积分面积,可以进行如下初始归属:
•一个羧酸质子。
•四个芳香质子。
•其余五个信号,来自十三个脂肪族质子。
由于布洛芬中只有一个羧酸质子,1可以指认为δH 11.9 ppm的信号。以δH 7.2 ppm为中心的四个芳香族质子的信号可归属于质子6和71。
为了进一步指定五种烷基信号,应在考虑其积分值和化学位移的同时分析其多重性。
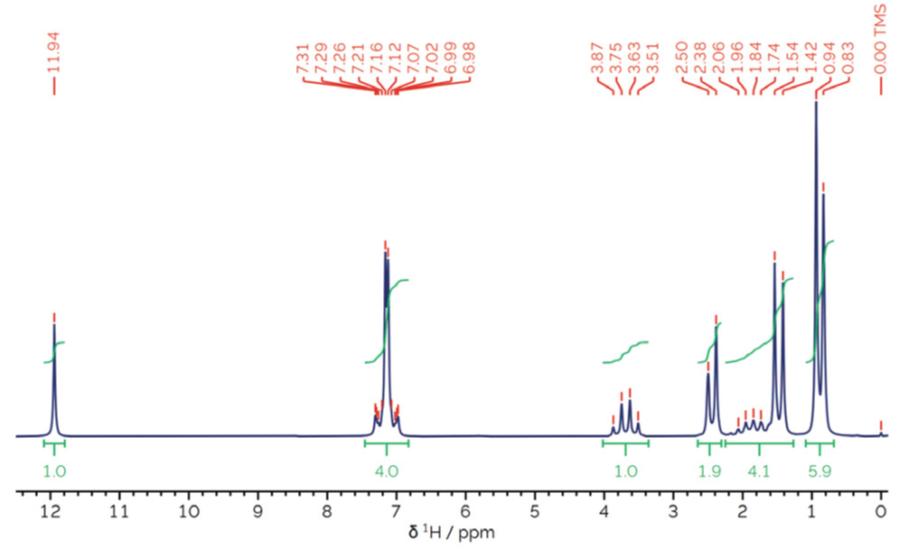
在简单的情况下,组成1H核磁共振信号的峰数,与相邻碳原子连接的质子数相关。因此,可以对剩余五个未归属信号进行如下推论。
δH 3.7 ppm处的信号由四个峰组成,并且积分为一个质子,这意味着一个CH基团与CH3基团相邻。布洛芬中唯一与此相一致的质子是3号。
δH 2.4、1.5和0.9 ppm处有三个信号,每个信号由两个峰(双峰)组成,表明它们紧邻一个CH基团。δH 0.9 ppm处的信号积分为六个质子,表明两个CH3基团,而两个甲基基团11,是布洛芬中唯一可能的质子。δH 2.4 ppm处的信号积分为两个质子,因此对应于与CH相连的CH2基团,与布洛芬的9相一致。δH 1.5 ppm处的剩余双重峰与δH 1.9 ppm处的多重峰(意味着具有复杂多重性的信号)重叠。对积分进行仔细检查,可以确定该双重峰对应于三个质子,因此是与布洛芬中的3位CH相连的CH3的信号。
通过排除过程,δH 1.9 ppm处的多重峰可归属于10位CH基团。该信号与两个CH3和一个CH2基团相连,可以解释这种复杂的耦合裂分模式。
虽然在这个案例中不需要指认质子核磁共振谱,但是从1H核磁共振谱中可以获得额外信息,以帮助归属信号。
当原子核之间发生耦合,导致在核磁共振波谱中观察到多重峰时,可以通过多重峰中各峰间的分离距离来测量耦合的大小(以Hz为单位)。由于耦合是一个常数,因此无论选择哪一对信号,都将测量到相同的值。这可以应用于核磁共振波谱中直接耦合的信号配对。例如,δH 3.7 ppm的四重峰被指认为3,其耦合常数3JHH为7.1 Hz,而δH 2.4、1.5和0.9 ppm的双重峰的耦合常数分别为3JHH 6.7、7.2和6.3 Hz,这表明δH 3.7ppm的信号与δH 1.5 ppm的信号相互耦合(已被指定为4)2。使用二维波谱可以避免这种可能耗时的测量和耦合配对过程,从而帮助谱峰归属。详见后文1H-1H COSY波谱内容。
碳-13核磁共振
质子是一个高旋磁比的原子核,天然丰度接近100%,是核磁共振波谱中“最好的”原子核。相比之下,碳的情况更为复杂。碳最丰富的同位素碳-12是没有核磁共振活性的。相反,碳核磁共振谱是测量碳-13的,但它只有1.1%的天然丰度,并且比质子的旋磁比低。由于碳-13只有质子可接受性的1/5870,因此需要更高的样品浓度和更长的测量时间。
碳-13核磁共振波谱如图3所示。碳谱看起来似乎比质子波谱简单,所有信号都显示为单个尖峰。这是因为所有的碳-质子耦合都通过质子去耦被去除了。
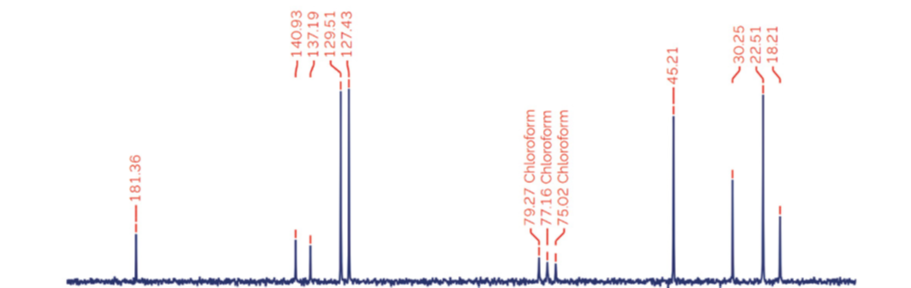
该谱被称为质子去耦碳-13核磁共振谱,简化为13C{1H} NMR波谱3。
然而,如前所述,布洛芬中有十种化学上独特的碳环境,但是其核磁共振谱图中仅观察到九种信号,表明两个信号重叠成为了一个单峰。如果这是一个质子核磁共振谱,通过评估峰的积分面积,可以很容易地识别任何重叠信号。但是质子去耦碳-13核磁共振波谱是一个例外,即峰(信号)的积分直接对应于产生该信号的原子核数目这一规则并不适用4。从13C{1H}核磁共振谱的信号强度可以推断出一些信息。一般来说,不直接与任何质子结合的碳原子(季碳)的信号强度,远低于直接与一个或多个质子结合的碳原子信号。
δC 181.4、140.9和137.2 ppm的信号,以及氘代氯仿溶剂产生的信号(1:1:1三重峰)都可以观察到这一点。
通过考虑这些碳信号的化学位移,可以将δC 181.4 ppm处的信号指认为羰基,从而归属为羧酸碳2。
而δC 140.9和137.2 ppm处的信号与芳香碳一致,因此归属为季碳5和8。
在芳香区的δC 129.5和127.4 ppm位置,两个更强的信号可被指认为芳香CH碳6和7。
碳-13核磁共振谱中的其余四个信号与烷基CHX碳一致,化学位移较低的信号可能对应末端甲基CH3基团。这些信号的彻底归属还需要其他额外的信息,而这些信息无法从简单的一维13C{1H}核磁共振谱中获得。
二维核磁共振波谱
到目前为止,只考虑了简单的一维核磁共振谱。然而,核磁共振波谱学的一大优势是可以使用种类多样的不同脉冲序列,从而获得不同的波谱。一类重要的脉冲序列是给出二维相关谱。这些情况下,可以通过检测到的交叉峰,对应相应一维波谱中观察到的信号之间的相互作用(例如通过J耦合)。以下示例演示了引入第二维度如何解决重叠带来的复杂问题,并显著简化了归属过程,实现了复杂分子的快速识别。
1H-1H相关谱
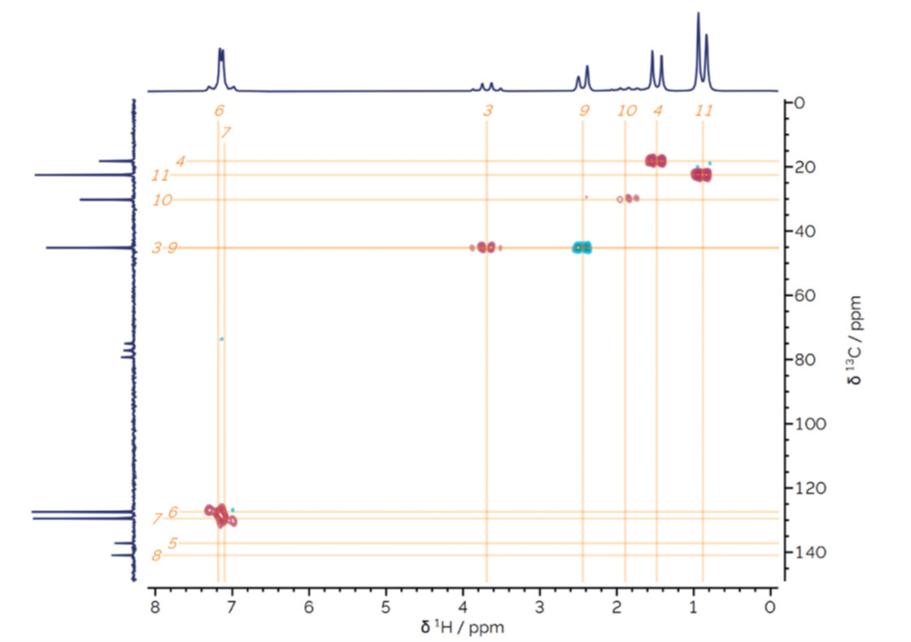
质子-质子相关谱(COSY)是要考虑的第一个二维谱,以布洛芬为例,如图4所示。
注意,在x和y轴上,显示了前面讨论的简单质子谱。实际的二维波谱由图4中红色的交叉峰组成。
作为同核相关谱,COSY谱沿对角线对称,信号直接耦合时出现非对角线交叉峰。通常,对于在一维谱中观察到J耦合的信号对,将会在COSY谱中观察到交叉峰。
在布洛芬案例中,4-CH3和3-CH可在COSY谱中观察到交叉峰。另外,在9-CH2、10-CH和11-CH3三个信号之间可以观察到交叉峰。这也是一个很好的例子,说明在一维谱中不能分辨的J耦合,或可在二维COSY谱中看到交叉峰,如9-CH2和11-CH3之间的四键相互作用。
1H-13C相关谱
除了像COSY这样的质子-质子相关实验外,观测质子-碳相关的脉冲序列也有助于信号的归属过程。最常用的两种是,允许观察质子-碳单键关联的且带多线编辑的异核单量子相干序列(HSQC-ME),以及允许观察质子-碳长程关联的异核多键相干序列(HMBC)。
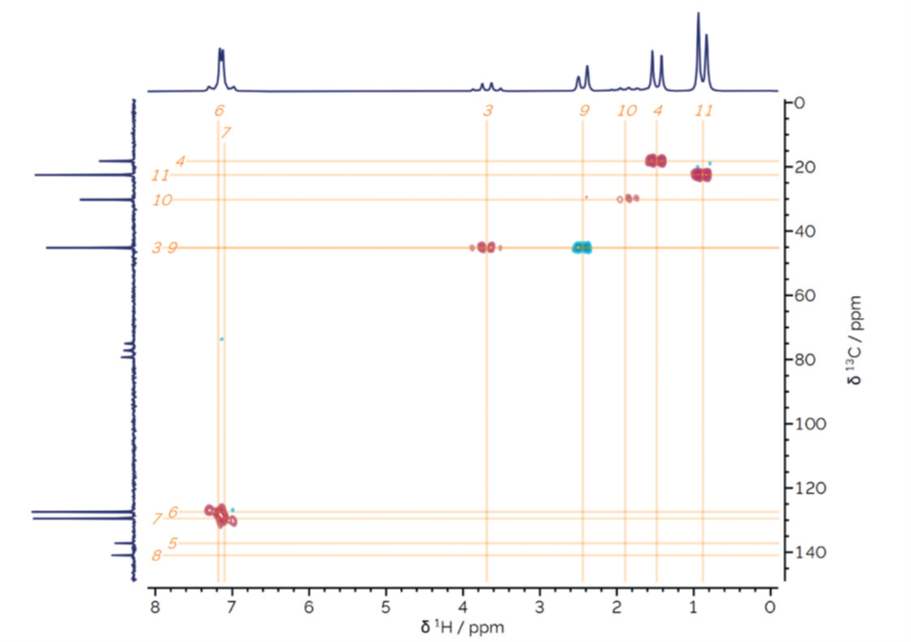
1H-13C HSQC-ME和1H-13C HMBC波谱(图5和图6)均在水平方向显示质子谱,而在垂直方向显示碳谱。图5中布洛芬HSQC-ME波谱的交叉峰对应于质子-碳单键相关。
该波谱还经过多线编辑,提供了CHX环境多重性的信息。CH和CH3以正相位的交叉峰显示(图5中为红色),CH2则以负相位的交叉峰呈现(图5中为蓝色)。
从HSQC-ME谱中应该注意到的第一件事是,它解释了为什么预期的十个碳信号,在一维13C{1H}谱中只能观察到九个信号。δC 45.2 ppm处的信号与两个质子信号相关:3-CH(δH 3.69 ppm)和9-CH2(δH 2.44 ppm),证实了直接连接到芳香环的两个碳原子,具有极为相近的13C化学位移。
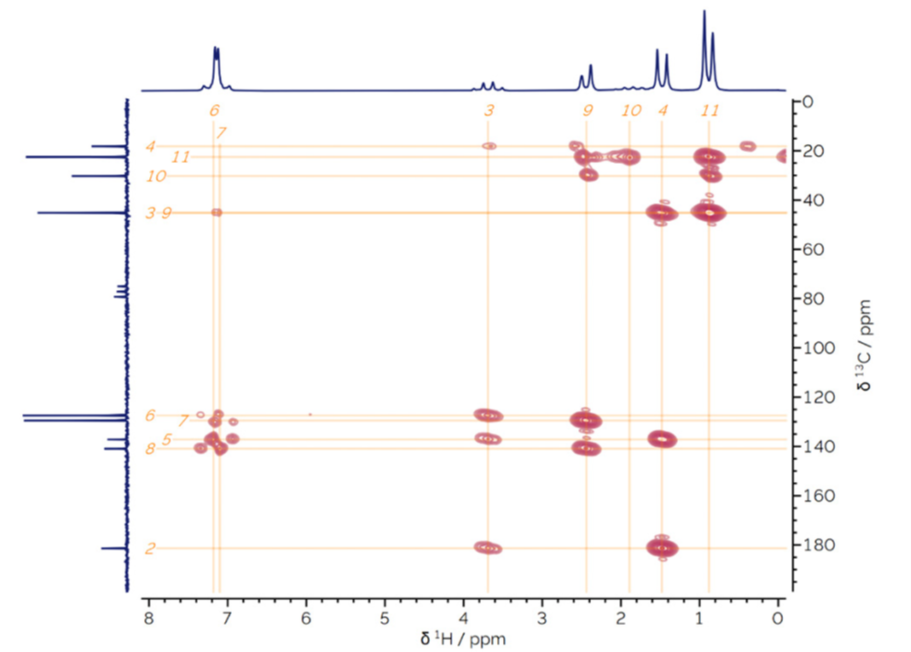
布洛芬的1H-13C HMBC波谱如图6所示。观察到的交叉峰对应于两键或三键的质子-碳关联。HMBC谱让布洛芬的完整结构归属/解析得以实现。
例如,在δH 3.69 ppm处的3-CH信号,与δC 127.4 ppm处的芳香族CH和δC 137.2 ppm处的芳香族季碳相关,可以分别确定这些信号的来源为6和5。通过对所有信号的系统分析,可以推断碳链的连接,并完成全谱归属/结构解析。
布洛芬谱图归属
通过分析所有这些波谱,可以在一维谱中实现信号的完全指认。布洛芬的质子和碳-13核磁共振谱的完整归属如下。
δH (60 MHz, 40°C, CDCl3): 11.94 (1H, s, 1-OH), 7.46 – 6.83 (4H, m, 6,7-C6H4), 3.69 (1H, q, 3JHH 7.1, 3-CH), 2.44 (2H, d, 3JHH 6.7, 9-CH2), 1.89 (1H, qt, 3JHH 6.7, 3JHH 6.3, 10-CH), 1.48 (3H, d, 3JHH 7.2, 4-CH3), 0.88 (6H, d, 3JHH 6.3, 11-CH3).
δC (15 MHz, 40°C, CDCl3): 181.36 (1C, s, 2-C=O), 140.93 (1C, s, 8-CH), 137.19 (1C, s, 5-CH), 129.51 (2C, s, 7-CH), 127.43 (2C, s, 6-CH), 45.21 (2C, s, 3-CH & 9-CH2), 30.25 (1C, s, 10-CH), 22.51 (2C, s, 11-CH3), 18.21 (1C, s, 4-CH3).
其它二维相关谱
COSY、HSQC和HMBC实验有助于NMR谱图的归属和化合物的解析,但它们并不是X-Pulse上仅有的二维脉冲序列。总相关谱(TOCSY)序列不仅可以观察COSY谱中可见的直接质子-质子耦合,还可以观察到通过自旋体系的间接质子-质子耦合。相关内容在我们的应用笔记 “自旋锁定:总相关谱(TOCSY)” 中进行了详细介绍和讨论。
核Overhauser增强谱(NOESY)可以显示出源自空间相互作用产生的交叉峰5,并可据此确定分子的三维结构。
总结
利用牛津仪器X-Pulse宽带台式核磁共振波谱仪,通过一系列一维和二维质子以及碳-13核磁共振脉冲序列,可以对多种小分子进行完整的结构归属/解析。当X-Pulse与X-Auto自动进样器结合使用时,对文中所有演示实验可实现一次性多达25个样品的自动信号采集。
 公安机关备案号31010402003473
公安机关备案号31010402003473